shRNA/miRNA/gRNA rAAV生产全方位服务,中等规模
特征:
-在大多数细胞类型(包括分裂细胞、非分裂细胞或原代细胞)中具有优异的基因传递效率。
-多血清型(AAV-1、AAV-2、AAV-3、AAV-4、AAV-5、AAV-6、AAV-8、AAV-9、AAV-DJ/8和AAV-DJ).
-持续转基因表达。
-诱导有效的基因沉默。
用于构建具有特定启动子和报告子的AAV顺式质粒的大型shRNA/miRNA/gRNA AAV顺式载体清单:
用于常规shRNA/miRNA/TuD-rAAV生产 |
单启动子shRNA/miRNA-AAV顺式载体
 |
双启动子shRNA/miRNA-rAAV顺式载体
 |
无促进者
巨细胞病毒
CAG
H1
U6
突触蛋白
UBC
EF1α
ALB(1.4)
载脂蛋白E/AAT1
卡姆基
ELA1
Enh358MCK
cTNT
GFAP
MBP
SST
待定
α-MHC
视网膜色素上皮
mIP1
tMCK |
|
无促进者
巨细胞病毒
CAG
H1
U6
突触蛋白
UBC
EF1α
ALB(1.4)
载脂蛋白E/AAT1
卡姆基
ELA1
Enh358MCK
cTNT
GFAP
MBP
SST
待定
α-MHC
视网膜色素上皮
mIP1
tMCK |
巨细胞病毒
CAG
H1
U6
突触蛋白
UBC
EF1α
卡姆基
cTNT
GFAP
|
表皮生长因子
招标书
mRFP
麦克赫里
番茄
涡轮GFP
eYFP
维纳斯
卢克
拉茨
|
用于CRISPR/Cas9 rAAV生产 |
单启动子CRISPR/Cas9 AAV顺式载体
 |
双启动子CRISPR/Cas9 AAV顺式载体
 |
无促进者
U6
H1
巨细胞病毒
CAG
CBH
突触蛋白
UBC
EF1α
ALB(1.4)
载脂蛋白E/AAT1
卡姆基
ELA1
Enh358MCK
cTNT
GFAP
MBP
SST
待定
α-MHC
视网膜色素上皮
mIP1
tMCK |
空的
CBH
U6
H1
sCMV
Syn
sEF1α
CK 0.4
cTNT
GFAP 0.6
斯辛
SST
待定
α-MHC
视网膜色素上皮
mIP1
tMCK
CBH |
Cas9
hCas9
SpCas9
hSpCas9
SaCas9
AsCpf1
hAsCpf1
ftCas9
st1Cas9
cjCas9
cdCas9
ciCas9
ncCas9
st3Cas9
nmCas9
mgCas9
nsCas9
|
无促进者
sCMV
U6
H1
tRNA
Syn
斯辛
sEF1α
卡姆基0.4 |
巨细胞病毒
sCMV
CBH
H1
U6
Syn
斯辛
sEF1α
卡姆基0.4
|
Cas9
hCas9
SpCas9
hSpCas9
SaCas9
AsCpf1
hAsCpf1
ftCas9
st1Cas9
cjCas9
cdCas9
ciCas9
ncCas9
st3Cas9
nmCas9
mgCas9
nsCas9
|
服务说明:
1.合成shRNA并克隆到AAV中顺式向量。
2.中等的AAV·HT的规模转染™ 将293个单元放入1xcell堆栈中。
3.收获rAAV粒子,然后通过先进的2xCsCl超离心纯化,获得rAAV载体的临床试验等级。
4.通过qPCR进行rAAV滴定。
我们提供的rAAV血清型:
AAV-1、AAV-2、AAV-3、AAV-4、AAV-5、AAV-6、AAV-7、AAV-8、AAV-9、AAV-PHP.B、AAV-PHP.eB、AAV-DJ/8和AAV-DJ.
所需材料:NCBI登入#,靶序列,验证的siRNA或验证的shRNA序列;miRNA加入、前miRNA、成熟miRNA或TuD(硬诱饵)miRNA。
周转时间:3.~4周。
可交付成果:>0.2ml超纯活体级大于1E+13 VG/mL时的rAAV矢量*.
我们为新客户提供折扣请求报价今天和我们在一起。
我们还提供截短的定制shRNA/miRNA AAV服务请求报价今天和我们在一起。
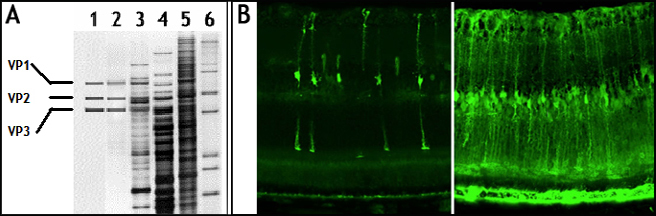
图1.来自不同来源的rAAV载体纯度和传染性的比较,显示通过我们先进的双CsCl超离心方法制备的超纯化和超传染性(接近临床试验级)rAAV载体。
A.来自不同来源的rAAV载体(每个通道的总1E+9 VG)在SDS-PAGE上解析,然后进行银染。通道1:GMP从CHOP制造的rAAV载体;通道2:通过我们先进的2xCsCl超离心方法制备的rAAV;通道3:来自BCM载体核心的rAAV;通道4:来自我们竞争对手“V”的rAAV;第5道:来自竞争对手“C”的rAAV;第6道:蛋白质标记。
B.通过先进技术制备的超级传染性rAAV载体双CsCl超离心. 左面板:我们的竞争对手“V”的rAAV9 GFP(总5E+9 VG)注入小鼠眼睛;右面板:rAAV-9-GFP(总5E+9 VG)通过高级2xCsCl纯化超离心注射到小鼠眼睛。
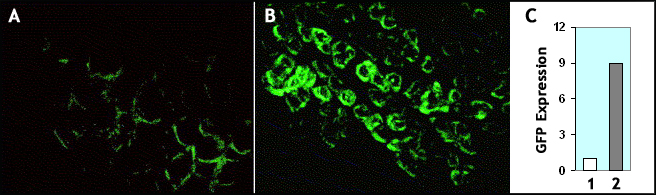
图2.来自不同来源的rAAV载体传染性的比较显示,通过先进的双CsCl超离心方法制备的超纯化rAAV具有超传染性。
将来自不同来源的rAAV1 GFP(总2E+9 VG)注射到小鼠肌肉组织中。注射后3周观察到GFP荧光。A.来自我们的竞争对手“V”的rAAV1 GFP;B.来自我们的预制rAAVs库存的rAAV1 GFP,通过高级纯化双CsCl超离心。定量数据显示,我们的超纯化rAAV(bar 2)的传染性是通过常规CsCl超离心制备的(bar 1)的约9倍。
*最终的病毒产量可能取决于转基因的性质。