188金宝慱亚洲体育APP下载188金宝搏下载手机版SignaGen Laboratories (SignaGen)是一家小型企业,专注于为生物医学研究社区开发和制造基因传递工具。基于我们独特的技术平台(专利申请,美国PTO # 61135606 & 072308), SignaGen成功开发了三种DNA/RNA转染试剂,并通过验证,以极高的效率和低细188金宝慱亚洲体育APP下载胞毒性轻松击败领先产品。更重要的是我们以合理的价格提供这些转染试剂。
1.生物降解聚合物(BDP)的合成:
这种BDP技术是我们正在申请专利的专有技术(美国PTO # 61135606 & 072308),它允许我们合成一种可生物降解的聚阳离子聚合物。与其他可用的阳离子聚合物如聚(l -赖氨酸)和聚(乙基亚胺)以及阳离子脂质体不同,这种新型聚合物有一个独特的主干,可以在基因载体卸载哺乳动物细胞内的DNA/RNA后被降解(图1),导致极低的细胞毒性。此外,该新型聚合物具有优异的核酸结合亲和力和高缓冲能力,满足优良基因载体的基本设计标准。体外DNA转染实验表明,这种新型生物可降解聚合物向HEK293T细胞传递DNA的效率是聚(乙基亚胺)的2到10倍。
图1.插图显示DNA转染与生物可降解聚合物
2.病毒蛋白模拟(vip)技术:
基因治疗是通过以治疗性基因为基础的药物的传递和表达来治疗人类遗传和获得性疾病的先进技术。使用安全、高效、可控的基因载体是临床基因治疗成功的前提之一。虽然病毒载体在基因传递中非常高效,但其潜在的安全性和免疫原性问题增加了其在临床应用中的风险。作为病毒载体的替代品,我们开发了一种独特的vip技术来模拟病毒核靶向肽序列。在此平台上,创建、合成和筛选了一系列模拟病毒(如慢病毒)的核靶向肽序列。经证实,结合脂质体DNA转染试剂,一系列这些模拟肽能够穿透细胞核孔,从而将DNA/RNA直接传递到细胞核(图2)。初步结果表明,几种模拟肽可以显著地——高达100倍,增强脂质体基因在多种哺乳动物细胞上的传递效率。有趣的是,在难以转染的非分裂细胞上观察到协同效应,为难以转染的细胞提供了一个潜在的非病毒核酸载体。
图2.显示vip模拟肽与脂质体转染试剂的协同效应
3.SCT技术:
细胞膜结构是脂质双分子层。脂质是两亲性的,因为它们有亲水的极性头指向外,疏水的部分形成核心。然而细胞膜表面是不均匀的(图3-I)。外周膜分子包括糖脂、糖蛋白、糖脂碳水化合物、跨膜蛋白、离子通道等也是膜的组成部分。此外,大多数细胞被其他几种类型的蛋白质修饰,这些蛋白质允许它们与其他细胞或细胞外基质结合。它们被称为细胞粘附分子(CAMs)。所有这些外周膜分子被称为细胞的“毛发”(图3-I),它们阻碍转染复合物(图3-II和III)进入和穿透细胞,损害转染复合物的内吞作用。这就是为什么常规的转染程序通常会导致低转染效率,尤其是在难以转染的细胞上。为了规避细胞毛发屏障,防止转染复合物内吞,我们开发了独特的转染试剂,具有独特的转染方案。我们的专利转染程序称为“剃毛细胞转染(SCT)”,在进行转染之前,细胞的毛发会被暂时剃光,然后再电镀剃光的细胞(图3-IV和V)。SCT技术允许转染复合物更容易、更有效地穿过和穿透细胞膜, leading to 3~15 times better efficiency than that on unshaved cells (Figure 3-V & VI). The SCT technology is extremely useful for transfecting the hard-to-transfect cells.
图3.一个演示如何剃光细胞转染技术的工作
4.转染介导的细胞毒性去除(TMCR)技术
研究人员在DNA/siRNA转染操作中经常遇到以下困境:高效的转染试剂通常具有很强的细胞毒性。有时毒性很强,转染后大量细胞被杀死。因此,研究人员不得不牺牲转染效率来获得相对健康的细胞。通过去除转染介导的细胞毒性,我们可以提供一种解决方案,在保持良好的细胞生存能力的同时,实现最大的转染效率。经过多年的研究,我们发现是转染复合物粘附在细胞表面导致细胞毒性(图4,上面板)。由于转染复合体的性质,不可能仅用转染后的介质改变来清洗复合体。我们开发了一个独特的产品的一些化学物质混合,使鸡尾酒(专利申请中,美国专利和商标局# 62375686)这是证实有效清除所有的转染细胞表面复杂的绑定到5分钟孵化在室温下(图4中,较低的面板),从而消除转染介导细胞毒性。
图4.展示转染介导的细胞毒性去除(TMCR)技术如何工作的插图
5.基于pH依赖的构象变化(PDCC)技术用于siRNA高效递送:
虽然脂质体或聚合物试剂通常能提供非常好的DNA传递效果,但它们不能有效地将siRNA驱动到哺乳动物细胞中。基于脂质体或聚合物的siRNA转染试剂性能较差可能与siRNA的阴离子段长度过短而无法与阳离子脂质或聚阳离子聚合物保持静电内聚有关。因此,siRNA脂质体或复合物在接触多阴离子细胞表面时太容易分裂。我们用特定的疏水基团修饰脂质体和聚合物,使其在生理pH条件下具有依赖于pH的构象变化(PDCC),并极大地稳定siRNA脂质体或复合物。PDCC技术同样重要的特性是,通过添加特定的疏水基团,siRNA脂质体或polyplex纳米颗粒可以控制成病毒样大小,从而大大提高siRNA转染效率。
图5.显示依赖pH值的构象变化(PDCC)技术如何工作的插图
6.广告。MAX™最大腺病毒产生技术:
广告。MAX™技术是通过基因改造病毒包装细胞、HEK293细胞和腺病毒穿梭载体或腺病毒基因组,最大限度地产生腺病毒。该专利技术的核心是基因工程的HEK293,在腺病毒包装过程中保持了腺病毒复制的完整性,同时显著抑制了病毒蛋白的表达。与腺病毒基因组中的跨元素结合,识别HEK293细胞的抑制盒,Ad。MAX™系统允许最大的腺病毒生产和最小的蛋白表达期间病毒包装。该系统对于包装带有毒性感兴趣基因(GOI)的腺病毒载体非常有用,否则该载体将在腺病毒复制和生成过程中杀死HEK293(图6),导致腺病毒产量显著减少。广告。MAX™技术最终允许研究人员构建腺病毒的所有基因(<7.5 kb)。
图6.展示广告如何。马克斯™技术是可行的
7.多途径产生超高滴度的超级传染性rAAV粒子:
与腺病毒不同,通过常规的rAAV生产程序获得高产量的rAAV相对比较困难。通过采用以下多种策略,我们成功地在超高滴度(高达1E+15 GC)下生产出超级传染性(感染能力比常规rAAV高约30倍)的rAAV颗粒。
- AAV·HT™包装电池:我们筛选了不同的HEK293细胞类型,并开发了一种高产菌株------AAV·HT™包装细胞,根据我们的验证数据,该细胞产生的rAAV颗粒比常规HEK293多10倍。
-修改rAAV cis载体:客户可以选择rAAV顺式载体,在转基因下游有一个截断的WPRE盒。与未加入WPRE的rAAV顺式载体相比,加入WPRE的rAAV顺式载体可产生约8倍的rAAV粒子。
—修改rAAV衣壳:rAAV衣壳在几个特定位点突变显著(约30倍)在体外&在活的有机体内)增强了rAAV的转导效率。客户可以选择用突变衣壳包装rAAV,以产生更具传染性的rAAV载体。
-包装双链AAV (dsAAV):双链AAV (dsAAV)也被称为自互补AAV (scAAV),被证实在这两种病毒中都能提供高达50倍的转导效率在体外和在体内.定制服务可以生成并打包感兴趣的基因到一个caav载体*。
-先进的双CsCl超离心协议:先进方案的主要特点是在装载到超离心前,经过3倍冻融循环和预沉淀步骤后,使用特殊配方的洗涤剂进行处理。该先进方案生产高纯度(临床试验级)和高传染性rAAV载体。看到图8获取详细信息。与传统协议的不同之处用粉红色标出。
图7。多途径产生超高滴度的超级传染性rAAV粒子
图8。概述和比较先进协议和常规协议。先进协议的差异用粉红色框定。
8.LentiMAX™慢病毒包装系统
慢载体与慢病毒包装混合物共转染后,包装细胞内部会产生大量的双链RNA (dsRNA)。dsRNA在细胞质中的积累将激活干扰素诱导的抗病毒防御途径。特别是当与dsRNA结合时,干扰素诱导蛋白激酶(PKR)被激活。激活的PKR磷酸化真核起始因子-2α (eIF-2α),从而阻断蛋白质合成起始。这导致了病毒RNA包装和翻译的抑制,从而影响了慢病毒特异性蛋白的稳定性和加工(图9上面板)。经证实,PKR抑制剂可显著提高慢病毒滴度。
基于这一原理,我们成功地开发了LentiMAX™慢病毒包装系统,通过在U6启动子下包含一个针对PKR特定变体的shRNA构建。在慢病毒包装过程中,通过引入PKR shRNA抑制PKR,我们从包装细胞上清液中获得了10^7 TU/mL的慢病毒,比传统包装方法高10倍(图9下图)。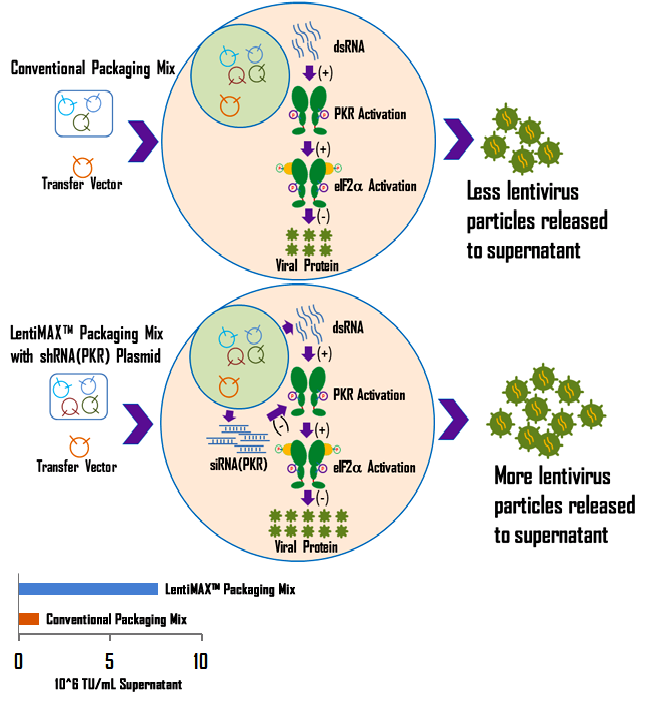
图9。展示LentiMAX™包装系统工作原理的插图。
*一些条款可能适用于定制的caav生产和包装服务。
